Sistemas dinámicos
2025 Workshop en Modelamiento de Sistemas Biológicos
Retroalimentación
Imaginemos dos genes, $Y$ y $X$, que producen un activador o un represor transcripcional capaz de unirse al sitio de unión del otro gen. Este diseño da lugar a cuatro configuraciones distintas, ilustradas en la Figura 1.
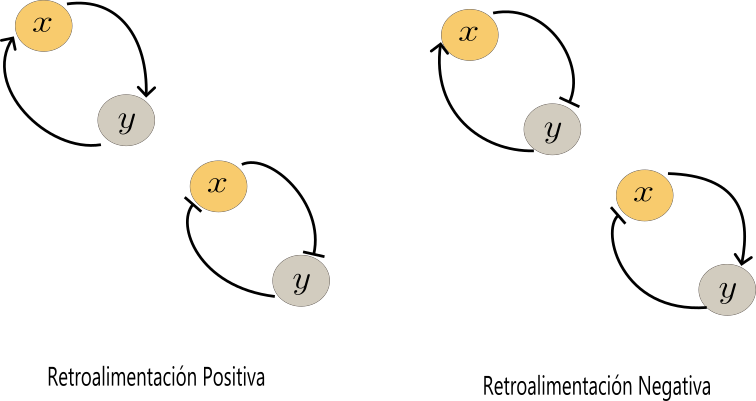
Los sistemas de retroalimentación (o feedback) son circuitos cerrados fundamentales para regular procesos celulares. Existen dos tipos principales. En la retroalimentación positiva, un proceso se amplifica a sí mismo, lo que permite generar respuestas rápidas o transiciones de estado. Por ejemplo, los linfocitos activados secretan citoquinas que promueven su propia proliferación (Wong et al, 2021). En cambio, la retroalimentación negativa ocurre cuando el producto de un proceso inhibe su propia producción, lo que estabiliza el sistema y lo hace resistente a perturbaciones externas. Un ejemplo común es la regulación de la glucosa: cuando sus niveles aumentan, el páncreas secreta insulina para restaurarlos a un rango saludable (Bich et al, 2020)
Mientras que la retroalimentación negativa mantiene el equilibrio, la positiva permite respuestas decisivas. Juntas forman la base de muchos comportamientos complejos en biología. Entre ellos destaca la biestabilidad , una propiedad asociada a la retroalimentación positiva que permite a una célula adoptar uno de dos estados estables alternativos (Angeli et al, 2004). Por su parte, la retroalimentación negativa puede generar oscilaciones, como las que se observan en los relojes biológicos o en circuitos génicos que regulan ritmos periódicos (François and Mochulska, 2024).
Sistemas multiestables
La biestabilidad y el toggle switch
El toogle switch es un circuito genético basado en la represión mutua entre dos genes. Fue introducido por Gardner, Cantor y Collins en el año 2000, quienes lo construyeron artificialmente en Escherichia coli (Gardner et al., 2000). En su forma más básica, el circuito consiste en dos genes que codifican represores, cada uno de los cuales inhibe la expresión del otro, como se muestra en la Figura 2.
Esta configuración genera un sistema no lineal con dos puntos de equilibrio estables, lo que permite que la célula se mantenga en uno de dos posibles estados de expresión: uno en el que el primer represor está activo y suprime al segundo, y otro en el que ocurre lo contrario.
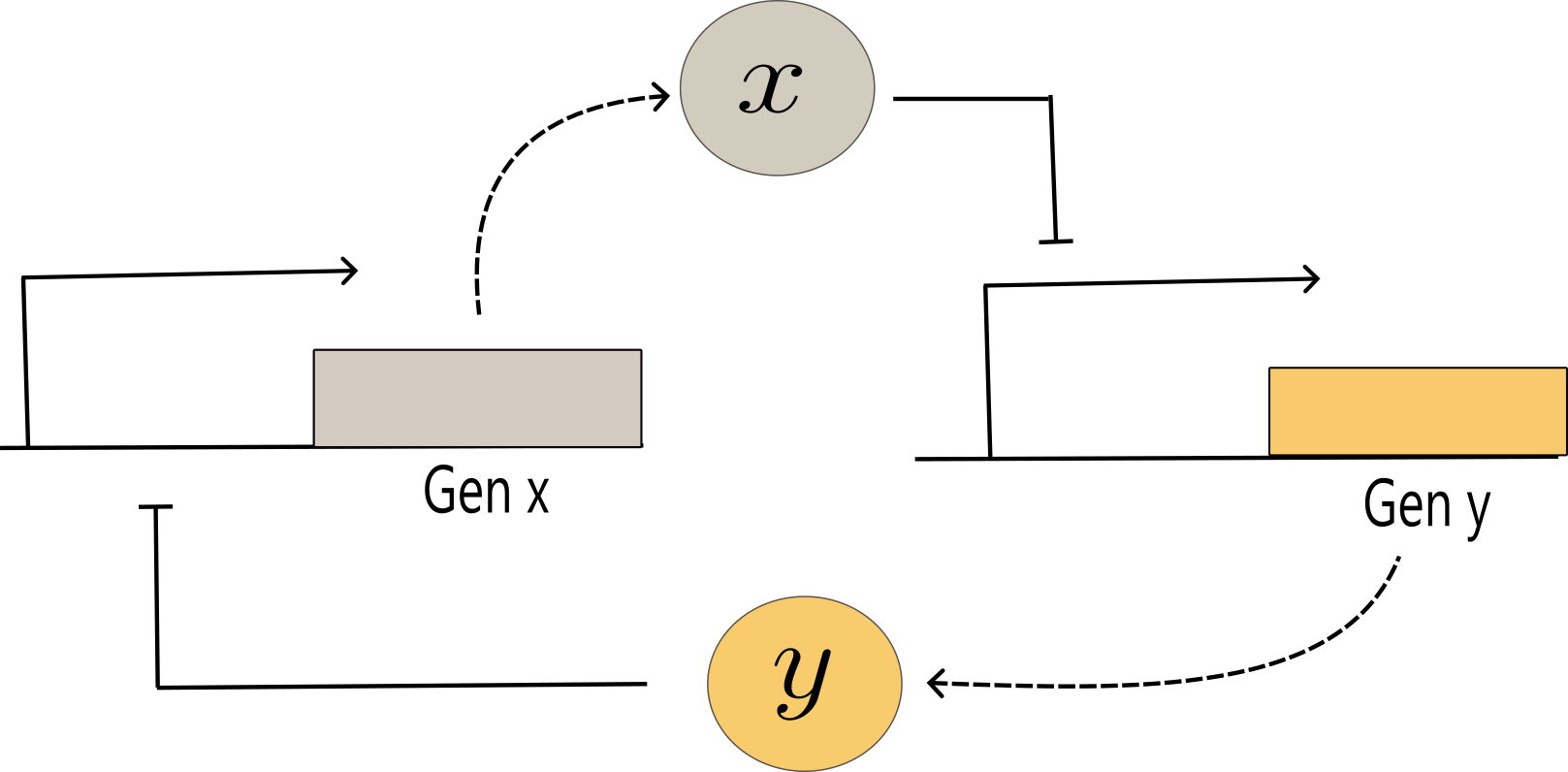
Llamemos $Y$ y $X$ a los genes que codifican a los represores transcripcionales. Los eventos bioquímicos que ocurren aquí estan dados por las siguientes reacciones químicas:
Asumiendo que la unión de los represores al sitio de unión en el promotor ocurre rápido (i.e., una suposición de cuasi-equilibrio) y que la represión sigue una cinética tipo Hill, las ecuaciones diferenciales que gobiernan el sistema son las siguientes:
Donde:
- $\alpha$: Tasa de producción [uM/h]
- $n$: cooperatividad
- $K$: constante de disociación [uM]
- $\delta$: tasa de degradación [1/h]
A la izquierda de la Figura 3 se muestran las trayectorias del toggle switch donde observamos como una especie reprime la expresión de la otra. Este comportamiento depende de las condiciones iniciales. Es decir, de la concentración con la que ambas especies iniciaron la reacción. A la derecha de la Figura 2, observamos como al disminuir las condiciones iniciales de la especie $X$, el sistema pasa de converger a un nivel alto de expresión de $X$ (color azul) a converger a uno bajo (colores rojizos).
La dinámica observada en el toggle switch sugiere que este sistema presenta biestabilidad, una propiedad fundamental en muchos sistemas no lineales. La biestabilidad se refiere a la existencia de dos estados de equilibrio estables: dependiendo del estado inicial del sistema o de perturbaciones externas, este puede estabilizarse en uno u otro estado, y permanecer allí incluso después de que la señal inicial desaparezca. Esta propiedad es esencial para comportamientos como la memoria en sistemas biológicos.
Una herramienta útil para estudiar la biestabilidad es el plano de fase, que nos permite visualizar cómo varía la concentración de una especie respecto a otra. En este plano, trazamos las nullclines de cada variable, es decir, las curvas donde la derivada temporal de esa variable es cero:
Las curvas donde $dX/dt = 0$ indica los valores de $X$ y $Y$ cuando están en equilibrio. Las intersecciones entre las nullclines corresponden a puntos de equilibrio del sistema, como se ve a la izquierda de la Figura 4. Este sistema presenta tres puntos de equilibrio, de los cuales dos son estables y uno inestable, por lo que decimos que hay biestabilidad: el sistema puede ''elegir'' entre dos estados estables dependiendo de su condición inicial.
A la derecha de la Figura 4, las líneas de colores representan las trayectorias del sistema cuando se inicia en esa condición inicial:
- Gris: Si se comienza en esta zona, se converge al punto de equilibrio 1.
- Naranja: Si se inicia en esta coordenada el sistema convergerá a punto de equilibrio 3.
- Si comenzamos exactamente en el punto de equilibrio 2, o en la zona de la frontera de ambas zonas, entonces el sistema converge al segundo estado estacionario.
Otra forma de entender esta propiedad es imaginándo que uno se encuentra observando una pelota sobre un paisaje montañoso, lleno de valles y cimas. La posición en la que se coloca la pelota representa la condición inicial del sistema, y el movimiento de la pelota representa cómo cambia ese estado con el tiempo (ver el dibujo de la Figura 5).
En esta analogía, un valle sería como un punto de equilibrio estable. Si colocamos la pelota en el fondo del valle, se quedará ahí, y aunque la empujemos ligeramente hacia un lado, regresará al fondo. Esto significa que pequeñas perturbaciones no alejarán al sistema de su estado original. Por otro lado, una cima sería como un punto de equilibrio inestable. Si se coloca la pelota justo en la cima, puede quedarse ahí, pero si se empuja, aunque sea un poco, caerá hacia uno de los lados y no volverá a la cima.

¿Cómo determinar la estabilidad de un punto de equilibrio?
Para determinar la estabilidad de un punto de equilibrio, se utiliza la matriz jacobiana del sistema evaluada en ese punto. Los pasos son los siguientes:
1. Definir la matriz jacobiana: Es una matriz que contiene las derivadas parciales de las ecuaciones del sistema respecto a las variables de estado. Por ejemplo, para un sistema con variables $X$ y $Y$, la matriz jacobiana $J$ está definida por
Donde $f_1$ y $f_2$ son las ecuaciones diferenciales del sistema.
2. Evaluar la matriz jacobiana en el punto de equilibrio: Sustituir las coordenadas del punto de equilibrio ($X_0, Y_0$) en la matriz jacobiana.
3. Calcular los valores propios (eigenvalores) de la matriz jacobiana:
- Si todos los valores propios tienen partes reales negativas ($\text{Re}(\lambda) < 0$), el punto de equilibrio es estable.
- Si al menos un valor propio tiene parte real positiva ($\text{Re}(\lambda) > 0$), el punto de equilibrio es inestable.
Si aplicamos estos pasos a nuestro modelo del toggle switch, observamos que, efectivamente, encontramos dos estados estables: uno que corresponde a la alta expresión de $Y$ y la baja expresión de $X$ (Figura 6, arriba a la izquierda), y el otro que corresponde a la alta expresión de $X$ y la baja expresión de $Y$ (Figura 6, abajo a la derecha). Para ver más detalles sobre como calcular estabilidad en sistemas multiestables, ver Technical Note #3.
Análisis de bifurcación
En muchos sistemas biológicos no basta con conocer cómo cambia el estado del sistema con el tiempo; también es fundamental entender cómo cambia el comportamiento general del sistema al modificar uno de sus parámetros. Imaginemos de nuevo la pelota sobre un paisaje con montañas y valles. La posición de la pelota representa el estado del sistema, y el relieve determina hacia dónde se moverá. Sin embargo, al variar un parámetro del sistema, el relieve puede modificarse; con esto pueden aparecer nuevos valles (nuevos equilibrios estables), desaparecer cimas (pérdidas de equilibrios inestables) o intercambiarse los roles de valle y cima (cambios de estabilidad). Este tipo de transformaciones en la estructura del paisaje se conocen como bifurcaciones.
En términos más formales, una bifurcación ocurre cuando un cambio en un parámetro del sistema provoca un cambio en el número o estabilidad de los puntos de equilibrio. Para estudiar esto, se utilizan los diagramas de bifurcación. En estos diagramas se representa el valor del parámetro en el eje horizontal y el valor de la concentración de una proteína en equilibrio en el eje vertical. Las curvas resultantes muestran cómo evolucionan los puntos de equilibrio conforme se varía el parámetro. En el caso del toggle switch, al variar la tasa de síntesis de la molécula $X$, vemos que con valores pequeños solo existe un punto de equilibrio; pero al aumentar dicha tasa, surgen dos nuevos (ver Figura 7).
Oscilaciones
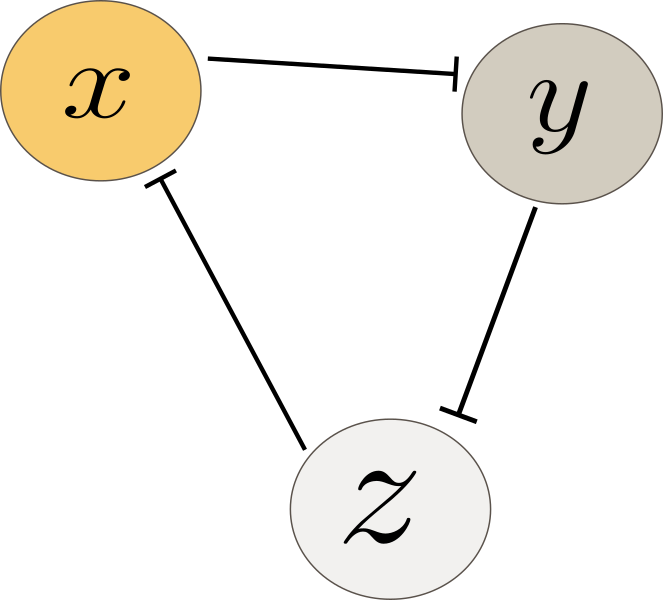
El mismo año en el que se publicó el toggle switch, Michael Elowitz y Stanislas Leibler diseñaron y construyeron un circuito genético llamado repressilator. Este representa uno de los primeros ejemplos de un sistema biológico sintético programado para exhibir un comportamiento dinámico no trivial: oscilaciones autosostenidas (Elowitz and Leibler, 2000). El circuito está formado por tres genes que se inhiben mutuamente en un ciclo de retroalimentación negativa, como se muestra en la Figura 8. Cada gen codifica para un inhibidor transcripcional que se une al siguiente gen en la cadena. Esta arquitectura genera un ciclo cerrado de retroalimentación negativa, lo cual, bajo las condiciones adecuadas, genera oscilaciones estables en los niveles de expresión de los tres genes. En otras palabras, las concentraciones de cada molécula suben y bajan de forma cíclica, generando oscilaciones.
Las reacciones químicas que describen al repressilator son las siguientes:
donde $f(z)$, $g(x)$ y $h(y)$ son las expresiones de Hill que dependen de la especie química dentro del paréntesis. Por simplicidad, estaremos asumiendo que todas las especies se degradan a la misma tasa $\delta$. De este modo, utilizando la ley de acción de masas, modelamos las reacciones químicas con las siguientes ecuaciones diferenciales:
Finalmente, si resolvemos las ecuaciones, observamos en la Figura 9 como las trayectorias de cada especie exhiben periodicidad.
Ahora que hemos confirmado la presencia de oscilaciones, podemos preguntarnos si es posible manipular las propiedades de esta señal. En particular, su amplitud y su frecuencia. Para ello, exploraremos el efecto de la tasa de producción ($\alpha$), el valor de cooperatividad (i.e., el coeficiente $n$ de la función de Hill) y la tasa de degradación ($\delta$).
Como se puede observar en la Figura 10, es posible ajustar la amplitud de las oscilaciones cambiando la tasa máxima de producción ($\alpha$), así como la frecuencia, cambiando la degradación de las especies químicas ($\delta$). Por otro lado, observamos que la cooperatividad ($n$) es necesario para generar oscilaciones. Si este es muy bajo, las oscilaciones resultan inestables y desaparecen con el tiempo; por el contrario, cuando es alto, las oscilaciones se estabilizan, formando un ciclo límite que puede observase en el plano de fase.
Formalmente, este es una trayectoria cerrada en el plano de fase hacia la cual tienden las soluciones de un sistema dinámico con el tiempo. Es decir, en vez de que las trayectorias terminen convergiendo a un valor constante, el sistema entra en un comportamiento periódico sostenido, donde las variables oscilan de manera regular y continua, sin necesidad de una señal externa.
En la Figura 11 observamos el plano de fase del repressilator. Existe un solo punto de equilibrio, alrededor del cual las trayectorias del sistema para diferentes condiciones iniciales giran. Si realizamos un análisis de estabilidad local, veremos que este tipo de comportamiento suele darse cuando encontramos eigenvalores ($\lambda$) complejos conjugados. Es decir, aquellos que tienen la siguiente forma: $\lambda = r \pm jw$, donde $r$ es la parte real, y $jw$ es la parte imaginario.
Lecturas recomendadas
[1] Gardner, T.S., Cantor, C.R. and Collins, J.J. (2000) ‘Construction of a genetic toggle switch in escherichia coli’, Nature, 403(6767), pp. 339–342. doi:10.1038/35002131.
[2] Elowitz, M.B. and Leibler, S. (2000) ‘A synthetic oscillatory network of transcriptional regulators’, Nature, 403(6767), pp. 335–338. doi:10.1038/35002125.
[3] Potvin-Trottier, L. et al. (2016) ‘Synchronous long-term oscillations in a synthetic gene circuit’, Nature, 538(7626), pp. 514–517. doi:10.1038/nature19841.
[4] Strogatz, S.H. (2019) Nonlinear Dynamics and Chaos: With applications to physics, biology, chemistry, and engineering. Taylor & Francis Ltd.